小编今天和大家分享的是初中化学中考图像题解题实用技巧,一定要学会喔!
图象题解题技巧
图象题是中考化学必考题型,常出现在单选最后一道题。
解决图象题需关注如下几个方面:
①起点;
②拐点;
③终点;
④曲线的变化趋势。
知识点睛
1.金属与酸反应的图象(以Mg、Al、Zn、Fe与稀盐酸反应为例)

技巧一:当其他条件相同时,金属的活动性越强,产生氢气的速度越快;
技巧二:等量金属与足量酸反应(金属耗尽)
技巧三:若等量酸与足量金属反应(酸耗尽),则产生氢气的质量相等。
(1)横坐标是时间,纵坐标是产生氢气的质量
①等量金属与足量酸反应(金属耗尽)
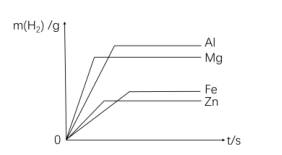
②等量酸与足量金属反应(酸耗尽)
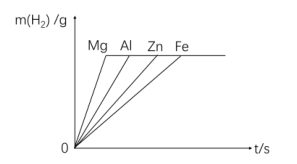
(2)横坐标是稀盐酸的质量,纵坐标是产生氢气的质量
等量金属与足量酸反应(金属耗尽)

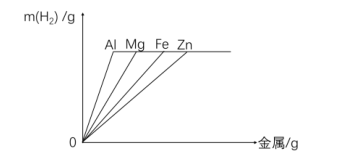
(3)横坐标是金属的质量,纵坐标是产生氢气的质量
等量酸与足量的金属反应(酸耗尽)
2.改变溶液pH图象题
技巧一:加水,只能改变溶液的酸碱度,不能改变溶液的酸碱性,即溶液的pH只能无限地接近7。
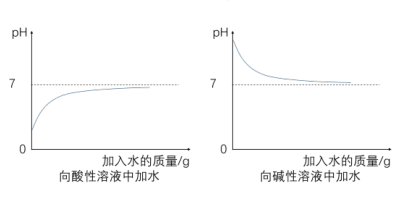
技巧二:酸碱互滴图象,重点体会反应过程与图象的关系。

3.金属和金属盐溶液反应过程中,固体质量或溶液质量的变化
技巧:根据金属相对原子质量或金属化合物相对分子质量来判断,例如

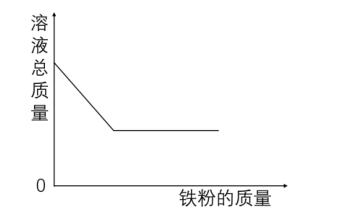
向一定量硫酸铜溶液中逐渐加入铁粉。观察方程式知:每56份质量的铁和160份质量的硫酸铜反应,就会生成64份质量的铜和152份质量的硫酸亚铁。由此可见,随着铁粉的加入,固体质量是增加的,溶液的质量是减少的。硫酸铜消耗完后,继续加入铁粉,固体质量持续增加,但溶液的质量将不会再改变。
图象如下所示:
4向混合溶液中加入某物质
(1)形如,

可表示为:
①向盐酸和氯化钙的混合溶液中滴加碳酸钠溶液(横坐标是碳酸钠溶液的质量、纵坐标是沉淀的质量)。提示:碳酸钠先消耗盐酸,待盐酸耗尽后,才与氯化钙反应生成沉淀。
②向稀硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液(横坐标是氢氧化钠溶液的质量、纵坐标是沉淀的质量)。提示:氢氧化钠先消耗硫酸,待硫酸耗尽后,才与硫酸铜反应生成沉淀。
③向氢氧化钠溶液和碳酸钠的混合溶液中滴加盐酸溶液(横坐标是盐酸溶液的质量,纵坐标是气体的质量)。提示:盐酸先消耗氢氧化钠,待氢氧化钠耗尽后,才与碳酸钠反应产生气体。
(2)向两种金属盐溶液中加入某金属,或向两种金属中加入某金属盐溶液。
技巧:“距离远、先反应”。
如:
金属活动性Fe>Cu>Ag。将铁粉放入含AgNO3和Cu(NO3)2的混合溶液里,将铁粉放入含AgNO3和Cu(NO3)2的混合溶液里,Fe先置换出Ag,再置换出Cu。同理,若将铁粉和铜粉放入AgNO3溶液里,Fe先置换出Ag,Fe耗尽后,Cu再置换出Ag。
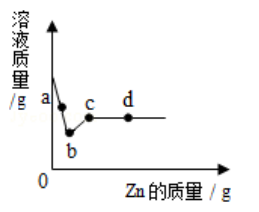
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示:
5特殊反应:向饱和氢氧化钙溶液中加入少量生石灰
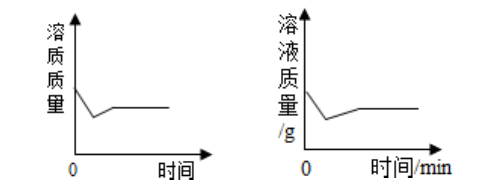
向饱和石灰水中加入少量的生石灰,生石灰和水反应生成氢氧化钙,水少了,原来的饱和溶液要析出一些氢氧化钙固体,又因为该反应放出热量,溶液温度升高,氢氧化钙的溶解度随温度的升高而减少,因此一段时间后析出氢氧化钙固体达到最大值,溶液质量达到最小值;随后随着温度的下降,一部分氢氧化钙固体又溶解,溶液质量又增加。
注意:自始至终,该溶液都是饱和溶液,但溶解度随温度的变化而变化!最初,溶解度随温度升高而降低,溶质质量分数减小,随后,随着温度恢复到初值,溶解度也恢复到初值,溶质质量分数也恢复到初值。

声明:本文信息来源于网络,由北京中考在线团队(微信公众号:BJ_zkao)整理制作,转载请注明来源和出处,否则追究法律责任。































